兩地藥監同日公告 9家藥品生產企業許可證被注銷,凸顯行業監管新常態
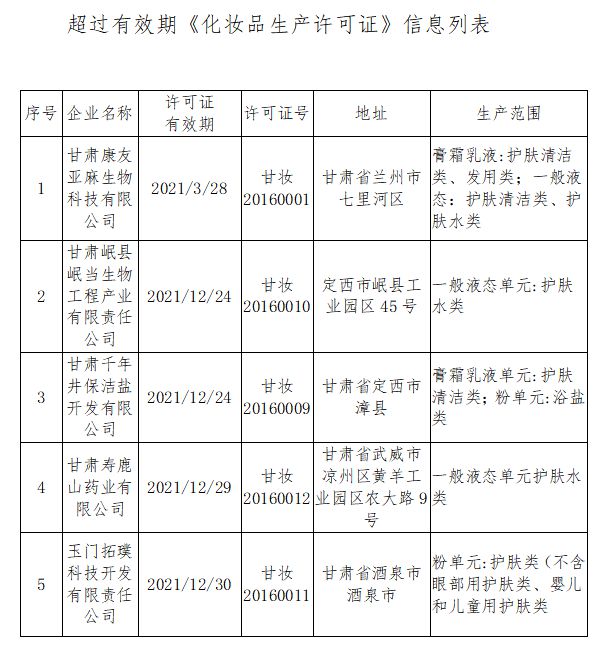
兩地省級藥品監督管理局同日發布公告,注銷了轄區內共9家藥品生產企業的《藥品生產許可證》。這一集中公告的舉措,迅速引發了醫藥行業及社會公眾的廣泛關注。這不僅僅是幾家工廠的“消失”,更清晰地傳遞出藥品監管持續趨嚴、行業優勝劣汰加速的強烈信號。
根據公告內容,此次被注銷許可證的9家企業,其經營范圍均包含“信息咨詢服務(不含許可類信息咨詢服務)”,但核心業務涉及藥品生產。許可證被注銷,意味著這些企業將不再具備合法的藥品生產資質,必須停止一切藥品生產活動。業內分析,企業退出的原因可能是多方面的:有的或是主動申請注銷,進行業務調整或戰略轉型;有的則可能是因長期停產、不符合現行《藥品生產質量管理規范》(GMP)要求、存在嚴重缺陷未能按期整改,或是在飛行檢查、產品抽檢中出現重大問題,從而被監管部門依法依規注銷許可。
此次兩地藥監局同步行動,釋放出明確的監管導向。它體現了監管的“穿透性”和“主動性”。監管部門不再被動等待,而是通過日常檢查、跟蹤回訪等方式,動態掌握企業生產狀態和質量體系運行情況,對名存實亡或無法保證質量安全的企業堅決清退,從源頭保障藥品安全。這有利于優化產業結構。注銷長期不生產、管理落后的企業產能,有助于將市場資源和監管力量更多集中于合規、優質的企業,推動整個醫藥產業向高質量、集約化方向發展。這也是對“信息咨詢服務”等非核心業務與主體生產業務分離管理的一種間接警示,強調企業必須將主要資源和精力集中于確保藥品生產這一核心生命線。
對于行業而言,這一事件是一個深刻的提醒。在醫藥監管法規日益完善、標準持續提高的背景下,“持證觀望”或“帶病運行”的空間已被極大壓縮。藥品生產企業必須將合規與質量置于首位,持續投入,確保生產全過程持續符合GMP要求。任何松懈都可能面臨出局的風險。
對于公眾而言,監管部門的此類“減法”實際上是藥品安全的“加法”。定期清理不具備條件的企業,如同為藥品安全的堤壩加固除險,能更有效地防范潛在風險,保障人民群眾的用藥安全有效。
隨著藥品監管科學的發展和新版《藥品管理法》的深入實施,類似的動態調整和許可證注銷可能會更加常態化、透明化。這預示著中國醫藥行業正步入一個以質量、創新和合規為核心競爭力的新發展階段,陣痛之后,將是更加健康、有活力的產業生態。
如若轉載,請注明出處:http://m.xiaovdiy.cn/product/78.html
更新時間:2026-04-30 17:20:42